- L’institut
- Un nouvel Institut Hospitalo-Universitaire
- Programme médico-scientifique
- Histoire de l’hématologie sur le campus de Saint-Louis
- Gouvernance de l’Institut
- Espace presse
- Nous contacter
- Notre actualité
- Lauréats de l’Appel à Projet Interne 2026
- Perspectives dans le traitement de l’aplasie médullaire
- Le Prix Olga Sain 2025
- Voeux de Hugues de Thé
- Portrait de Vincent Bansaye, Professeur à l’Ecole polytechnique
- Nous soutenir
- Nous rejoindre
- Vous êtes
- Patients et proches
- Être soigné et accompagné
- Nos services cliniques
- Nos soins de support
- Traitements anti-cancéreux
- Notre recherche clinique sur les leucémies
- Devenir patient expert
- Découvrir l’Institut
- Chercheurs
- Recherche
- Essais cliniques
- Découvrir l’Institut
- Professionnels de la santé
- Adresser un patient
- Notre recherche clinique
- Découvrir l’Institut
- Un nouvel Institut pour la lutte contre la leucémie
- Histoire de l’hématologie sur le campus de Saint-Louis
- Industriels
- Découvrir l’Institut
- Recherche translationnelle
- Donateurs
- Nous soutenir
- Découvrir l’Institut
- Soin
- Prise en charge des patients
- *Leucémies Aiguës Myéloïdes
- *Leucémies Aiguës Myéloïdes – Traitement intensif
- *Leucémies Aiguës Myéloïdes – Traitement non intensif
- *Allogreffe de cellules souches hématopoïétiques (CSH)
- *Leucémies aiguës lymphoblastiques
- *Traitement LAL – Chimiothérapie
- *Traitement par CAR-T cells
- *Allogreffe de cellules souches hématopoïétiques (CSH)
- *Néoplasies myéloprolifératives (NMP)
- *Traitement de la Polyglobulie de Vaquez ou Thrombocytémie Essentielle
- *Traitement de la Myélofibrose
- *Syndrome myélodysplasique (SMD)
- *Leucémies Myéloïdes Chroniques (LMC)
- *Réaction du greffon contre l’hôte (GVH)
- Réunions de concertation pluridisciplinaires ouvertes
- Nos services cliniques
- Hôpital Saint-Louis – Service Hématologie Adultes
- Hôpital Saint-Louis – Service Hématologie Greffe
- Hôpital Saint-Louis – Service de Pharmacologie et Investigations Cliniques
- Hôpital Saint-Louis – Service Adolescents Jeunes Adultes
- Hôpital Saint-Louis – Unité ambulatoire d’hémato-oncogénétique
- Hôpital Saint-Louis – Service Hématologie Séniors
- Hôpital Robert-Debré – Service d’Hématologie et immunologie pédiatrique
- Hôpital Necker – Service d’Hématologie Adulte
- Hôpital Cochin-Port Royal – Service Hématologie Clinique
- Hôpital Avicenne – Service Hématologie Clinique et Thérapie Cellulaire
- Nos laboratoires de biologie médicale
- Laboratoire d’hématologie biologique, Michaela Fontenay
- Laboratoire d’hématologie biologique, Jean Soulier
- Unité fonctionnelle de génétique moléculaire, Hélène Cavé
- Laboratoire d’hématologie biologique, Vahid Asnafi
- Informations pour les patients
- *Soins de support
- *Accompagnement psychologique des patients atteints de leucémies et de leurs proches
- *Transfusion sanguine
- *Grossesse et leucémie aiguë
- *Diagnostic
- *Hémogramme (NFS), Myélogramme ou Biopsie Ostéo-Médullaire (BOM)
- *Hématopoïèse
- *Analyses génétiques pour le diagnostic de votre maladie
- *Gestes en hématologie
- Traitements anti-cancéreux
- *Chimiothérapie anti-cancéreuse
- *Thérapie ciblée
- *Allogreffe de cellules souches hématopoïétiques (CSH)
- *Participer à un essai clinique
- *La fertilité et la leucémie aiguë
- Recherche
- Nos équipes de recherche
- Equipe de Hugues de Thé – Pathologie Moléculaire
- Equipe de Raphael Itzykson – Médecine de précision fonctionnelle des leucémies
- Equipe de Michaela Fontenay – Hématopoiese normale et pathologique
- Equipe de Françoise Pflumio – Niche, cancer et radiation dans l’hématopoïèse
- Equipe de Sylvie Méléard – Evolution de populations et système d’interactions de particules
- Equipe de David Michonneau – Immunologie translationelle en immunothérapie et hématologie
- Equipe de Lina Benajiba – Identification et ciblage des régulateurs extrinsèques des hémopathies myéloïdes
- Equipe de Karl Balabanian – Niches lymphoïdes, chimiokines et syndromes immuno-hématologiques
- Equipe d’Alexandre Puissant – Bases moléculaires du développement des leucémies aiguës myéloïdes
- Equipe de Stéphane Giraudier – Hémopathies myéloïdes chroniques, microenvironnement & recherche translationnelle
- Equipe de Diana Passaro – Leucémie et dynamiques de la niche
- Equipe de Camille Lobry – Contrôle génétique et épigénétique de l’hématopoïèse normale et maligne
- Equipe de Jean Soulier – Aplasie et leucémies secondaires
- Equipe de Sylvie Chevret – Biostatistiques et épidémiologie clinique
- Equipe de Emmanuelle Clappier – Base génomique de la leucémie aiguë lymphoblastique B
- Equipe de Vahid Asnafi – Différenciation lymphoïde normale et pathologique
- Equipe de Matthieu Duchmann – Evolution clonale et plasticité des cellules leucémiques [LEAP]
- Nos plateformes technologiques
- Notre recherche clinique sur les leucémies
- Participer à un essai clinique
- Portail de transparence
- eTHEMA : La cohorte des patients atteints de leucémies
- Enseignement
Accueil *Allogreffe de cellules souches hématopoïétiques (CSH)*Allogreffe de cellules souches hématopoïétiques (CSH)
...Comprendre une allogreffe
L’allogreffe de moelle consiste à remplacer la moelle osseuse malade par celle d’un donneur compatible.
Une allogreffe de CSH (Cellules Souches Hématopoïétique) permet de :
- rétablir une production normale et efficace des cellules sanguines par la moelle osseuse (hématopoïèse)
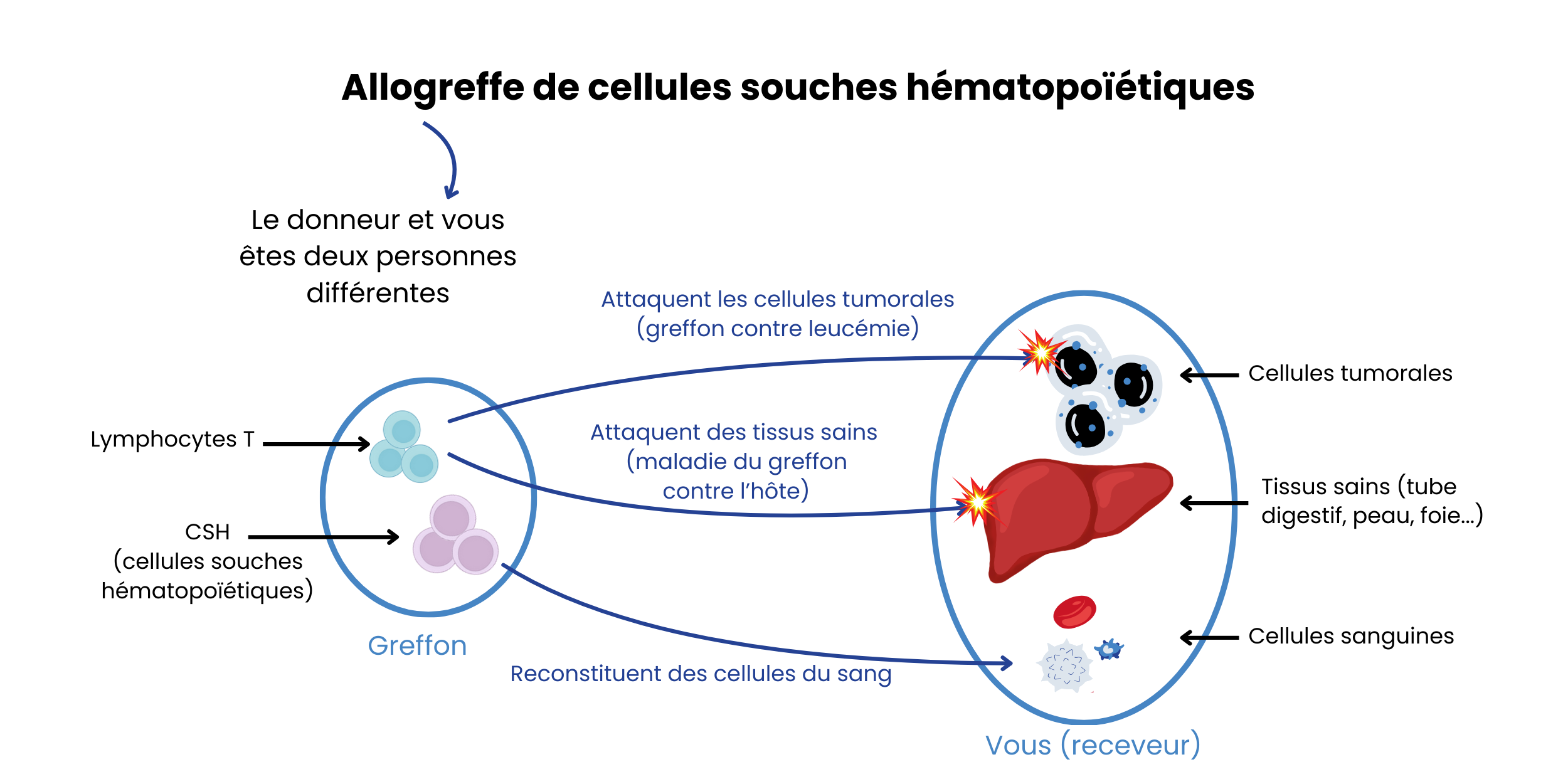
- vous apporter un nouveau système immunitaire pour lutter contre votre maladie. C’est l’effet du greffon contre la leucémie = GVL.
L’allogreffe de CSH consiste à éviter le risque de rechute de la maladie hématologique.
Elle est indiquée :
- lorsque la moelle osseuse ne produit plus correctement les cellules sanguines (comme une aplasie médullaire sévère)
- lorsqu’il existe une maladie cancéreuse du sang ou de la moelle osseuse (leucémie aiguë, lymphome, myélodysplasie, etc.)
- dans le cadre de certains déficits immunitaires ou maladies génétiques (comme la drépanocytose)
L’indication la plus fréquente est la leucémie aiguë.
Déroulement
Le donneur est choisi en fonction de sa compatibilité. Il peut s’agir :
- d’un frère ou d’une soeur : donneur géno-identique (100% compatible, 1 chance sur 4) ou haplo-identique (50% compatible, 1 chance sur 2)
- d’un parent ou enfant : donneur haplo-identique (50% compatible, 1 chance sur 2)
- d’un donneur sur fichier volontaire des donneurs de moelle osseuse : donneur non apparenté
- d’une ou de deux unités de cordon placentaire (unité de sang placentaire) conservée(s) dans une banque de sang placentaire.
Ce bilan permet de s’assurer que vous êtes prêts à recevoir une allogreffe.
Il comprend :- une prise de sang
- une analyse de la moelle osseuse (myélogramme) selon la pathologie pour laquelle vous êtes traité
- une échographie cardiaque
- des examens de la fonction respiratoire (EFR)
- un scanner du corps entier
- une consultation dentaire avec radiographie de toutes les dents (panoramique dentaire)
L’hospitalisation pour la greffe se fait dans une chambre à flux pour diminuer le risque d’infections, notamment à champignons.
Elle dure environ 6 à 8 semaines.
Un cathéter central doit être posé à l’entrée pour permettre :
- l’hydratation
- l’administration de la chimiothérapie
- si nécessaire la nutrition parentérale ou des antibiotiques
C’est une chimiothérapie pouvant parfois être associée à une radiothérapie (irradiation corporelle totale).
But du conditionnement : détruire les cellules de la moelle osseuse (myéloablatif), permettre la prise de la greffe et éviter le rejet (immunosuppresseur) et obtenir un effet anti-tumoral.
Son intensité varie en fonction de l’indication de l’allogreffe, de l’âge et d’éventuelles pathologies associées : les doses peuvent être fortes (conditionnement myéloablatif) ou plus modérées (conditionnement d’intensité réduite).
Effets secondaires :
- aplasie,
- perte temporaire des cheveux,
- troubles digestifs (nausées, diarrhées, douleurs abdominales, perte d’appétit),
- ulcérations douloureuses dans la bouche (mucite)
- hémorroïdes
- impact potentiel sur la fertilité
Correspond au jour 0 du parcours de greffe.
Le greffon est administré par le cathéter, de façon similaire à une transfusion sanguine.
Le greffon peut provenir :
- de la moelle osseuse (le donneur est prélevé au bloc opératoire)
- des cellules souches périphériques (les cellules souches du donneur sont prélevées dans le sang grâce à une machine dite de cytaphérèse)
- ou d‘unités de sang placentaire (après décongélation)
Un traitement immunosuppresseur après la greffe permet d’éviter la maladie du greffon contre l’hôte (GVH) et éventuellement le rejet du greffon. Il dure au moins 3 mois. Les modalités et la durée du traitement immunosuppresseur après la greffe dépendent du type de greffe, de la compatibilité du donneur et de l’indication de greffe.
Conséquence du conditionnement, car les cellules du greffon ont besoin de temps pour migrer dans la moelle osseuse et progressivement fabriquer les différentes cellules du sang (globules blancs, globules rouges, plaquettes).
Elle dure environ 2 à 4 semaines.
Durant l’aplasie, des transfusions de globules rouges et/ou de plaquettes peuvent être nécessaires, et les défenses immunitaires sont affaiblies (augmentation du risque d’infections).
Peuvent être nécessaire :- des antibiotiques ou des traitements antifongiques (contre les champignons) et antiviraux.
- une alimentation est dite protégée afin de limiter les risques d’infection
- en cas de mucite ou de perte d’appétit, un support nutritionnel par une sonde naso-gastrique ou par le cathéter (alimentation parentérale).
Suivi
Le suivi peut durer jusqu’à environ 3 mois après la greffe, au rythme d’1 fois par semaine.
L’objectif de ce suivi étant de vérifier l’absence de besoin de transfusion, dépister d’éventuelles complications (infections, maladie du greffon contre l’hôte) et ajuster le traitement immunosuppresseur (dosage).
Un bilan complet est effectué environ 3 mois après la greffe.
L’objectif de ce bilan est de vérifier la stabilité de votre état. Une nouvelle échographie cardiaque et des examens de la fonction respiratoire sont réalisées. Un contrôle du myélogramme est également programmé
Si tout est satisfaisant, le cathéter est retiré.
Un suivi à long terme est maintenu à vie, en consultation, par le médecin qui vous avait expliqué l’allogreffe. Les consultations seront progressivement espacées.
La reprise de la scolarité ou de l’activité professionnelle peut s’envisager 3 à 6 mois après la greffe si votre état le permet.
La reprise du plan vaccinal sera initiée à partir de 4 à 6 mois après la greffe mais peut parfois être retardé selon la reconstitution de vos défenses immunitaires.
Un suivi pluriprofessionnel peut vous être proposé en fonction des besoins avec d’autres spécialités (dermatologie, pneumologie, ophtalmologie, gynécologie) et d’autres médecins spécialistes ou professionnels de santé (psychologue, diététicien…).
Complications spécifiques
En plus des complications en lien avec la chimiothérapie de conditionnement et l’aplasie, certaines sont spécifiques à l’allogreffe :
- Le rejet de greffe ou non prise du greffon est rare et peut nécessiter une deuxième greffe.
- La maladie du greffon contre l’hôte (ou GVH) survient lorsque les cellules du donneur reconnaissent vos tissus (notamment la peau, le tube digestif et le foie) comme étrangers et les attaquent. Les formes peuvent être légères, sévères voire mortelles. Cette réaction se produit fréquemment car il y a toujours des différences entre le donneur et le receveur. Pour l’éviter ou diminuer son intensité, des traitements immunosuppresseurs sont prescrits. Si cela ne suffit pas, d’autres immunosuppresseurs sont prescrits pour diminuer la réactivité du greffon contre le receveur (corticostéroïdes). La maladie du greffon contre l’hôte peut être aiguë (elle se manifeste juste après la greffe) ou chronique (elle se manifeste tardivement, jusqu’à 2 ans après la greffe).
- La maladie veino-occlusive est une complication rare mais potentiellement grave causée par l’obstruction de petites veines du foie. Elle peut provoquer des douleurs abdominales, une prise de poids et des difficultés pour la transfusion de plaquettes. Des traitements pour éviter cette complication vous seront administrés dès le début du conditionnement et jusque 3 mois après la greffe.
Nos projets de recherche
Plusieurs protocoles peuvent vous être proposés pour améliorer les modalités de greffe au sein des services du Pr Peffault et du Pr Boissel.
Il vous sera également proposé de faire partie du registre anonyme national (SFGMTC) et européen (EBMT) des greffés de CSH qui permettent d’harmoniser les pratiques et d’améliorer la prise en charge des patients recevant une allogreffe.Suivez nos actions en vous inscrivant à la lettre d'information de l’institut
- *Leucémies Aiguës Myéloïdes
- Découvrir l’Institut
- Recherche translationnelle
- Notre recherche clinique
- Essais cliniques
- Être soigné et accompagné
- Un nouvel Institut Hospitalo-Universitaire